- A+

过去十年来,在不同的医疗需求、快速的市场扩张和监管体制改革的推动下,中国药企十分重视药物研发的创新。尽管中国目前是全球第二大医药市场,但大多数中国制药企业仍处于创新药物研发的萌芽阶段。
最近,来自复旦药学院的邵黎明教授团队在Nature Reviews Drug Discovery上发文,分析了中国本土药企20强与跨国药企研发和创新能力的差别,为人们了解中国医药产业在创新研发方面的全球地位提供了清晰的认识。中外药企差距临床阶段产品
2012~2021年的10年期间,跨国制药公司20强中的大多数药企有超过15种获批药品,上市的药品总数为313种。相比之下,中国本土20强药企大多没能超过5个,而且10年间仅有31个产品得到了批准, 见图1。
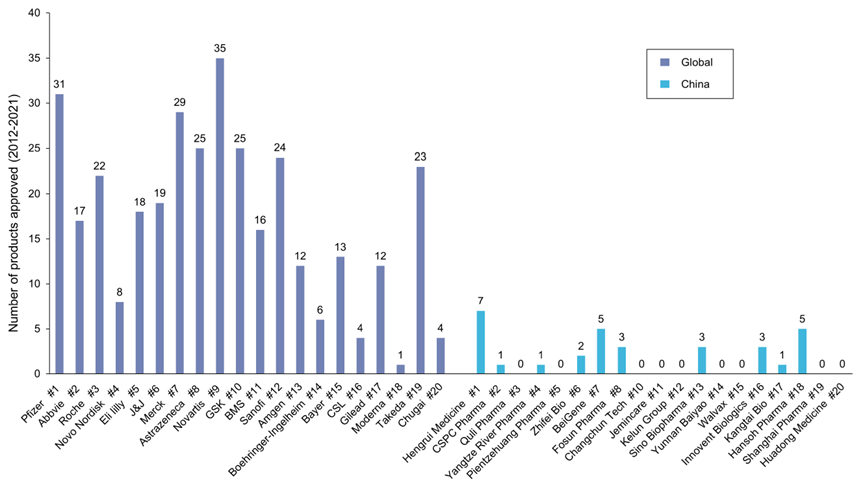
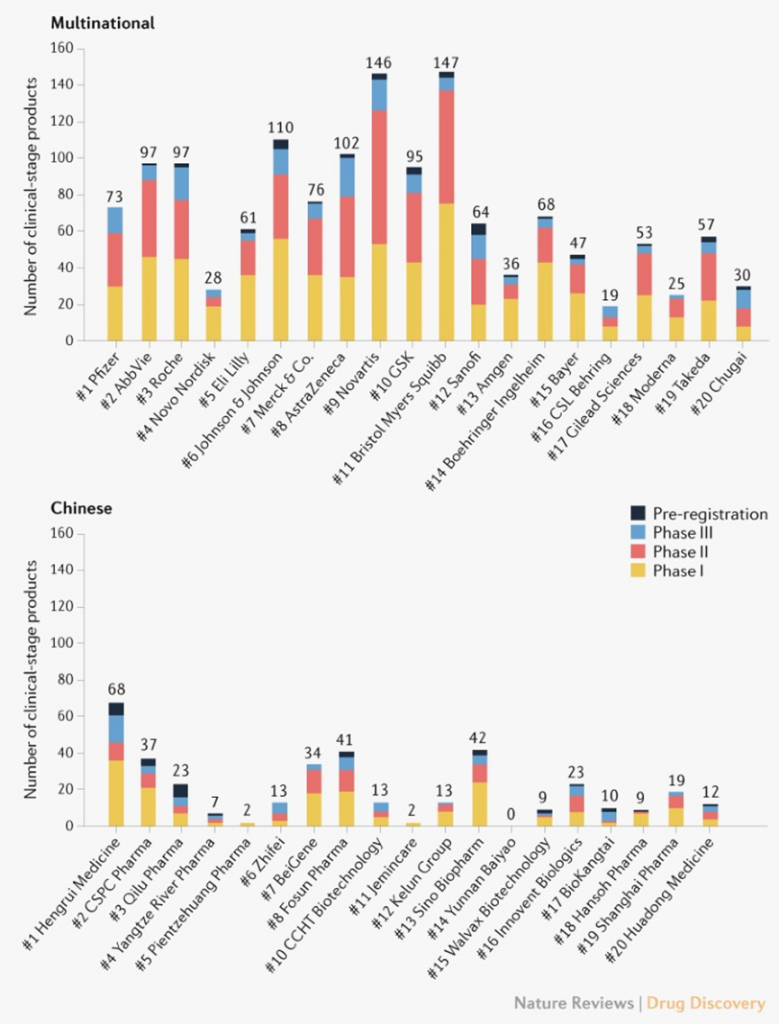
中国和跨国药企的临床阶段产品数量差距则相对较小(图2 ),下面两个因素促成了中国药企临床阶段产品的快速增长。
其一,江苏恒瑞医药和CSPC医药集团等领先的传统医药企业目前正将重心从生产制造转向创新药物的研发,恒瑞医药的临床阶段产品数量达到了全球前20家药企的中位数水平(66个);其二,领先的创新研发驱动型制药企业成为中国医药产业的中坚力量,如百济神州、复星医药和中国生物制药业等。
治疗领域
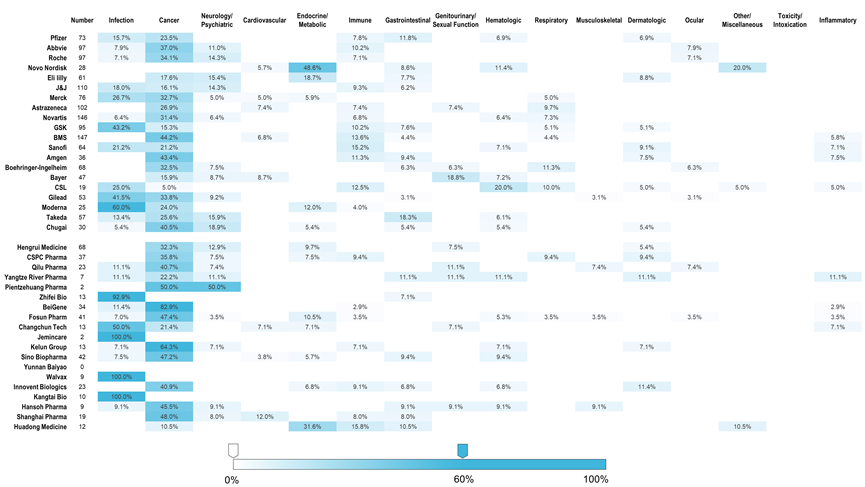
顶级跨国制药公司拥有比中国公司更多样化的产品管道,他们瞄准多个治疗领域。相比之下,许多中国公司往往专注于单一的治疗领域。在研发重点方面,肿瘤领域在中国和跨国制药企业中均处于领先地位。在排名前20的跨国药企中,有12家药企的临床组合中的肿瘤治疗是其最大的治疗领域,占所有候选药物的20~40%。
对于中国企业而言,排名前20的药企中,有9家的肿瘤药物占比在40%以上,其中百济神州的占比最高为83%(图3)。传染病、神经病学、免疫学和呼吸系统领域的候选药物在跨国公司的管道中比在中国公司更常见。
新靶点和作用机制
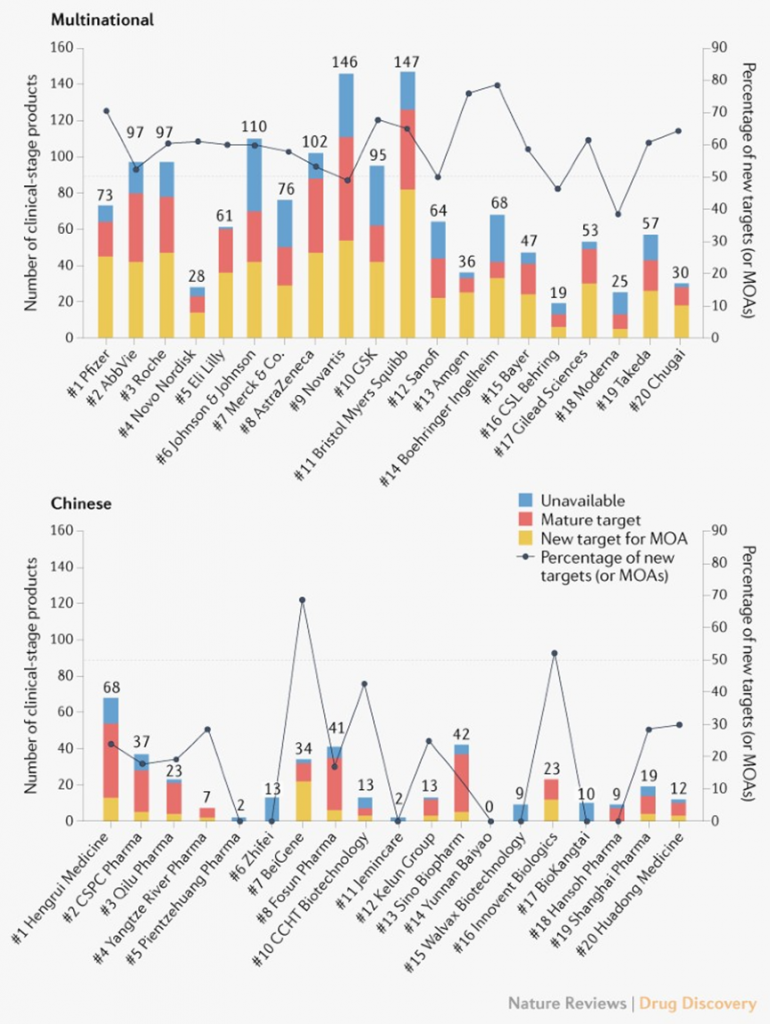
为了量化评估药企的研发和创新能力,这里考察了具有新靶点或者新的作用机制(MOA)的临床阶段产品的百分比,根据批准的药物是否使用类似的靶点,评估了跨国药企和中国本土药企管道中的相对创新水平。
数据表明,跨国药企20强的绝大多数超过50 %的药物在其管道中都有新的MOA (图4)。相比之下,中国药企前20强中,仅有百济神州和信达生物超过一半的产品拥有新型MOA。对于其他中国本土药企来说,新型MOA的比例不到30%。恒瑞医药虽然在临床阶段的产品数量上具有竞争力,但仅有24%的候选药物拥有新型MOA。
最后,根据每个药企在临床阶段管道中使用新型MOA的产品超过或少于50%,以及临床阶段产品超过或少于中位数66个的简单标准,使用4个象限的二维图表来评估每个公司在创新研发中的定位,从而量化评估药企的研发和创新能力。
前20家跨国药企中有9家落在右上象限,说明他们的新型MOA比例较高,临床阶段产品数量较多,而中国前20家药企大部分落在左下象限,新型MOA较低和临床阶段产品数量较少,唯一的例外是百济神州、信达生物和恒瑞医药。
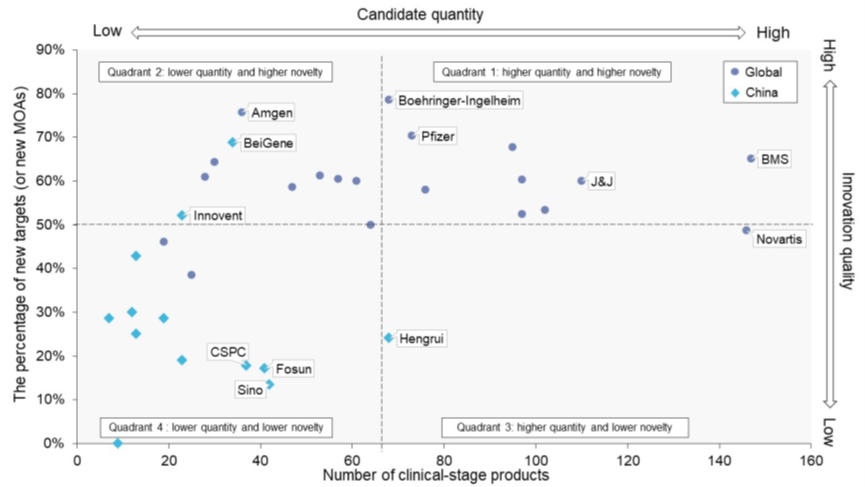
大多数中国顶级医药公司在投资新靶标或机制方面的滞后,反映了本土药企在创新研发方面相对保守。尽管如此,创新研发的格局可能会随着时间和战略管道规划而重新洗牌。中国制药企业提高创新能力,从左下象限晋升到右上象限,有两条可能的路径:
其一,可以效仿百济神州和信达生物,依托公司现有的研发能力和优势,拓展原创性研究。在短期内,这种方法可能不会产生大量的新候选药物,但长此以往,这将使中国本土药企能够在相对新颖的赛道与跨国药企竞争。
其二,那些长期专注于仿制药的中国制药公司,可以尝试利用其充足的资金和优良的管理能力,开发更多风险小的创新型制剂。





